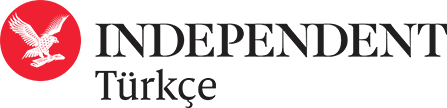Obezite ve yüksek yağlı beslenmenin, kanser henüz ortaya çıkmadan yıllar önce karaciğer hücrelerini sessizce “yeniden programlayarak” tümör riskini artırabileceği ortaya çıktı. Cell dergisinde yayımlanan yeni bir araştırmaya göre, bu süreç kansere yol açan genetik mutasyonlar ya da gözle görülür tümörler mutasyonlar ortaya çıkmadan çok önce başlıyor.
Günümüzde yağlı karaciğer hastalığı, obezite oranlarındaki artışla birlikte dünya nüfusunun üçte birinden fazlasını etkiliyor. Metabolik hastalıklarla ilişkili karaciğer kanseri vakaları ise küresel ölçekte hızla artıyor. Buna rağmen hekimler, yağlı karaciğer hastalığı olan hangi hastaların kansere ilerleyeceğini öngörebilecek güvenilir araçlara hâlâ sahip değil.
Araştırma, kanser riskinin yalnızca DNA’da biriken hasarlardan değil, uzun süreli metabolik strese (özellikle uzun süreli yüksek yağlı diyet) verilen bir “biyolojik stres yanıtı” üzerinden de gelişebileceğini gösteriyor. Bu durum, kanserin klinik olarak teşhis edilebilecek aşamaya gelmeden çok önce, hücresel düzeyde sessizce şekillenmeye başlayabileceğine işaret ediyor.
Araştırmada yer alan Harvard Üniversitesi’nden Prof. Dr. Ömer H. Yılmaz, konu hakkında şu bilgiyi verdi:
Araştırma tümörler fiziksel olarak oluşmadan çok önce karaciğer hücrelerinde saptanabilen belirgin "biyolojik stres imzaları" olduğunu gösteriyor. Örneğin HMGCS2 geninin azalması veya SOX4'ün artması gibi. Bu moleküler değişimler, gelecekte yapılacak testlerle riskli hastaları tümör oluşumundan yıllar öncesinde belirleyen bir erken uyarı sistemi olarak kullanılabilir.
Bu kapsamlı araştırma Massachusetts Institute of Technology (MIT), Massachusetts General Hospital (MGH) ve Harvard Tıp Fakültesi bünyesinde gerçekleştirildi. Çalışma, eş-birinci yazarlar Constantine N. Tzouanas, Jessica E.S. Shay ve Marc S. Sherman ile kıdemli yazarlar Wolfram Goessling, Ömer H. Yılmaz ve Alex K. Shalek öncülüğünde yürütüldü.
Araştırmacılar, yüksek yağlı diyetle beslenen fareleri 6, 12 ve 15 ay boyunca takip ederek, karaciğer hücrelerinin zaman içindeki dönüşümünü ayrıntılı biçimde inceledi.
Bu süre, farelerin yaşam süresi dikkate alındığında insanlarda yıllara yayılan obezite ve yağlı karaciğer sürecine karşılık geliyor.
Bu uzun takip boyunca bilim insanları, karaciğer dokusunu yalnızca mikroskop altında incelemekle yetinmedi.
Tek hücreli ve mekânsal genomik teknikler kullanılarak, her bir karaciğer hücresinin hangi genleri ne zaman aktif hale getirdiği, hücrenin dokunun neresinde bulunduğu ve zaman içinde nasıl değiştiği ayrıntılı biçimde haritalandı.
Amaç, kanser ortaya çıkmadan önce hücre düzeyinde nelerin değiştiğini adım adım izlemekti.
Sonuçlar çarpıcıydı. Obezite ve yüksek yağlı beslenmenin yol açtığı uzun süreli metabolik stresin, karaciğer hücrelerini sessizce yeniden programlayarak kanser riskini yıllar öncesinden artırabileceği ortaya çıktı. Normalde vücudu temizleyen, enerjiyi düzenleyen ve hayati maddeler üreten karaciğer, uzun süreli yağlı beslenme altında bu temel görevlerini giderek kaybetmeye başladı.
Cell dergisinde yayımlanan araştırmanın en dikkat çekici yönlerinden biri, bu değişimlerin kanser geliştikten sonra değil, kanserden çok önce başlaması oldu. Henüz tümör olmayan karaciğer dokusunda bile, ilerleyen aylarda ve yıllarda tümör oluşumuyla güçlü biçimde ilişkili gen programlarının aktif hale geldiği saptandı.
Bu bulgu, kanser riskinin yalnızca DNA’da biriken mutasyonlardan değil, hücrelerin uzun süreli strese verdiği biyolojik yanıttan da kaynaklanabileceğini gösteriyor.
Sonuçlara göre karaciğer hücreleri zamanla olgun kimliklerini ve temel metabolik işlevlerini kaybediyor. Bu süreçte HNF4A ve HMGCS2 gibi karaciğerin sağlıklı işleyişinde kritik rol oynayan metabolik düzenleyiciler baskılanırken, WNT sinyal yolu gibi stres ve hayatta kalma mekanizmaları aktif hale geliyor. Bu moleküler değişim, hücrelerin metabolik strese dayanmasını sağlıyor; ancak aynı zamanda aylar hatta yıllar sonra tümör gelişimi için uygun bir zemin hazırlıyor.
Kronik metabolik stres karaciğer hücrelerini kansere yatkın bir duruma itiyorsa, bu süreç kanser ortaya çıkmadan önce durdurulabilmesiyle ilgili olarak Prof. Dr. Yılmaz, şu bilgiyi verdi: “Çalışma, bu sürecin kalıcı genetik mutasyonlardan ziyade, hücrelerin yağlı beslenmeye karşı geliştirdiği metabolik bir uyum süreci olduğunu ortaya koyduğu için sürecin durdurulabileceğini öngörüyor. Beslenme alışkanlıklarının değiştirilmesi veya keşfedilen bu stres mekanizmalarını, örneğin keton metabolizmasını, hedefleyen yeni ilaçlarla, hücrelerin kansere giden hatalı programlaması engellenebilir.”
Araştırmacılar, farelerde saptanan bu biyolojik “ön-kanser” imzalarının, yağlı karaciğer hastalığı ve karaciğer kanseri olan insanlardan alınan doku örneklerinde de görüldüğünü belirledi. Üstelik bu imzaları taşıyan hastaların daha kötü sağkalım oranlarına sahip olduğu ortaya çıktı. Bu da çalışmanın yalnızca deneysel değil, insan hastalıklarıyla doğrudan ilişkili olduğunu gösteriyor.
Araştırma, hücresel stres yanıtlarının bu erken uyarı sinyalleri için bir temel oluşturabileceğini düşündürüyor. Bu da beslenme değişiklikleri, yaşam tarzı müdahaleleri ya da yeni geliştirilecek ilaçlarla, tümörler ortaya çıkmadan önce sürecin tersine çevrilip çevrilemeyeceği sorusunu gündeme getiriyor.
Prof. Dr. Yılmaz, bu konuda şunu söylüyor:
Araştırma, karaciğer hücrelerinin kronik stresi "epigenetik bir hafıza" olarak kaydettiğini, ancak tümör oluşmadan önceki evrede bu sürecin geri çevrilebilir olduğunu düşündürüyor. Doğru zamanlama ile yapılacak müdahalelerin, bu "kötü hafızayı" silerek hücreleri sağlıklı işlevlerine döndürebilecek ve sürecin kalıcı hale gelmesi önleyebilecek.
Araştırma, kanserle mücadelede odağın yalnızca tümörleri tedavi etmeye değil, onları ortaya çıkaran uzun vadeli biyolojik süreçleri erken dönemde anlamaya ve önlemeye kayması gerektiğine işaret ediyor.
Araştırmacılar, benzer stres yanıtı programlarının yağlı karaciğer hastalığı ve karaciğer kanseri olan insanlardan alınan örneklerde de görüldüğünü ve bu biyolojik imzaların hastalarda daha kötü sağkalım oranlarıyla ilişkili olduğunu belirledi. Bulgular, metabolik hastalıklarla ilişkili karaciğer kanserinin neden dünya genelinde hızla arttığına dair yeni ipuçları sunuyor.
Öte yandan, yağlı karaciğer hastalığına yönelik yeni ilaçlar ve tarama stratejileri geliştiriliyor. Bu da hangi hastaların gerçekten yüksek risk altında olduğunun belirlenmesini her zamankinden daha acil hale getiriyor.
Bulguların, yağlı karaciğer hastalığı olan bireylerin nasıl izlenmesi ve hangi hastaların daha yakından takip edilmesi gerektiği konusunda yeni bir yol haritası sunabilmesi konusunda Prof. Dr. Yılmaz, “Bu çalışma, sadece karaciğer yağlanması olan hastalar ile hücresel düzeyde kanser yoluna girmiş hastaları birbirinden ayırt edebilecek yeni biyolojik kriterler sunuyor. Hekimler bu bulguları kullanarak, hücresel stres ve kanser öncüsü sinyalleri taşıyan yüksek riskli hastaları belirleyip onlar için çok daha sıkı bir takip ve tedavi planı oluşturabilirler” diye konuştu.
*Bu içerik serbest gazeteci veya konuk yazarlar tarafından hazırlanmıştır. Bu içerikte yer alan görüş ve ifadeler yazara aittir ve Independent Türkçe'nin editöryal politikasını yansıtmayabilir.
© The Independentturkish