Kaybedilen bir uzuv neden geri gelmezken, bazı canlılar bunu başarabiliyor?
Bu soru yıllardır bilim dünyasının en temel problemlerinden biri.
Yeni bir çalışma ise tartışmayı kökten değiştirebilecek bir yanıt ortaya koyuyor: mesele genler değil, oksijen olabilir.
Science dergisinde yayımlanan araştırma, kurbağalarda gerçekleşen uzuv yenilenmesi ile farelerde gerçekleşmeyen süreçleri karşılaştırdı.
Sonuç net: fark, genetik eksiklik değil; hücrelerin oksijeni algılama biçimi.
Araştırmaya göre oksijen seviyesinin düşürülmesi ya da HIF1A proteininin stabilize edilmesi, memelilerde erken evre yenilenme programlarının tetiklenmesini sağlayabiliyor.
Araştırma, rejeneratif tıpta kök hücre ve biyomühendislik odaklı yaklaşımlardan, doğrudan biyolojik “anahtarları” hedef alan yeni bir döneme geçişin sinyalini veriyor.
En kritik nokta ise şu: çalışma, memelilerde yenilenmenin neden başlamadığını açıklayan ilk net ve test edilebilir mekanizmalardan birini ortaya koyuyor.
Yenilenme yeteneği kaybolmadı, baskılanıyor
Memelilerin aslında yenilenme kapasitesine sahip olabileceğini, ancak bu kapasitenin aktif olarak baskılandığını düşündürüyor.
Max Planck Enstitüsü Tübingen’den Dr. Can Aztekin, memelilerde yenilenmenin tamamen ortadan kalkmadığını, belirli koşullar altında yeniden tetiklenebilecek bir süreç olabileceğini söyledi.
İnsanların da farelerle benzer şekilde “yüksek oksijen hassasiyeti” taşıdığı ve bu nedenle yenilenmenin evrimsel olarak korunmuş bir mekanizma üzerinden kontrol altında tutuluyor olabileceğini belirten Aztekin, şunları söyledi:
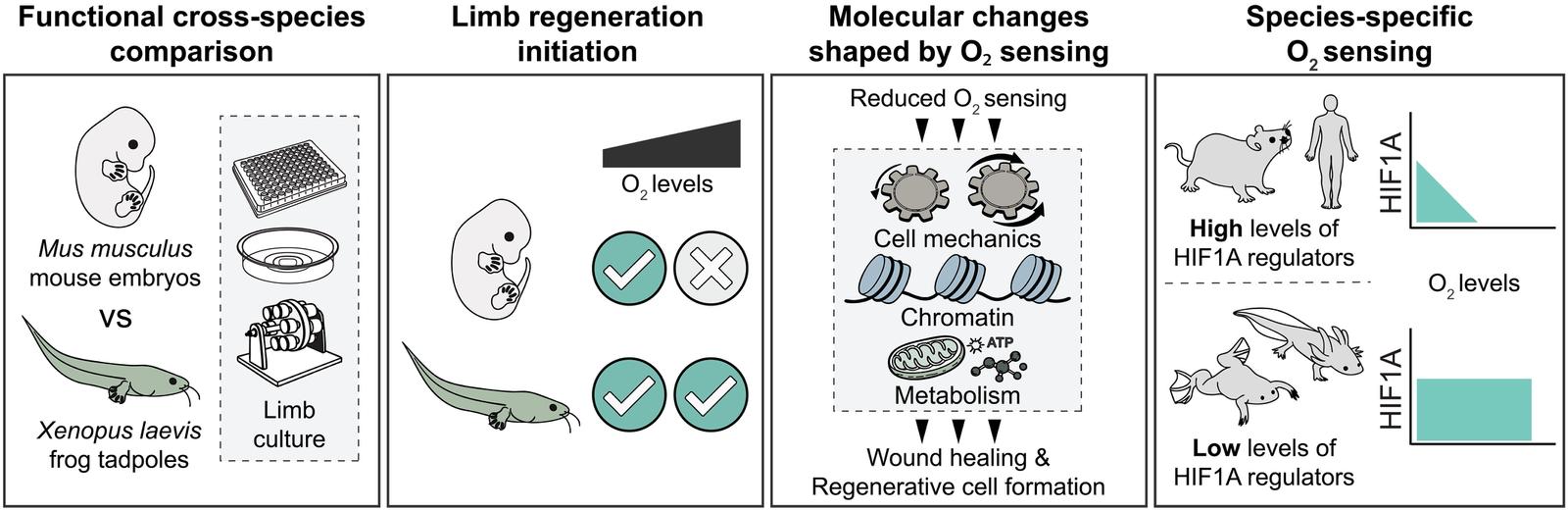
Çalışmamız, memelilerde uzuv yenilenmesini sınırlayan temel faktörlerden birinin hücrelerin oksijeni algılama ve buna yanıt verme biçimi olduğunu gösteriyor. Oksijen seviyesini düşürdüğümüzde, kesilen yaranın kapanması, doku mekanikleri, metabolizma ve epigenetik gibi yenilenmenin başlaması için gerekli birçok sürecin etkilendiğini görüyoruz.
Buna karşılık, kurbağa iribaşlarında hücrelerin oksijen algısı memelilere kıyasla daha farklı ve daha az hassas. Bu hayvanlar, hepimizin soluduğu atmosferik oksijen seviyelerinde (yüzde 20) ya da daha yüksek oksijen koşullarında (yüzde 60) bile bu değişimleri memeliler kadar güçlü şekilde algılamıyor. Bu sayede hücreler, yenilenmeyi başlatmaya daha elverişli bir durumda kalabiliyor.
Yani sorun memelilerde bir genin eksikliği değil; oksijenin hücresel düzeyde nasıl algılandığı ve bu sinyalin erken yenilenme programını normal koşullarda başlatamaması.
Kritik eşik: Oksijen
Araştırmanın merkezinde oksijen yer alıyor. Hücrelerin oksijen seviyesine verdiği yanıt, yenilenme sürecini doğrudan etkiliyor.
Çalışma, oksijen algısının metabolizma, doku mekanikleri ve epigenetik yeniden programlama gibi süreçlerle bağlantılı olduğunu ortaya koyarak, vücudun “yenilenme moduna” nasıl geçebileceğini açıklıyor.
Bu durum, rejeneratif tıpta uzun süredir odak noktası olan kök hücre ve biyomühendislik yaklaşımlarının ötesinde, hücresel çevrenin ve metabolik durumun doğrudan hedeflenebileceğini gösteriyor.
Hücrelerin oksijen algısındaki değişimin yalnızca basit bir çevresel tepki olmadığını belirten Aztekin şunları söyledi:
Hücreler oksijen seviyesindeki değişimleri büyük ölçüde HIF1A adlı bir gen üzerinden algılar. Normalde atmosferik oksijen koşullarında HIF1A proteini aktif değildir. Buna karşılık düşük oksijen koşullarında aktifleşir.
Aktif HIF1A, hücrelerin hayatta kalmasını ve uyum sağlamasını desteklemek için metabolizma, hücre mekanikleri ve epigenetik düzenleme gibi birçok süreci yeniden programlar. Bizim bulgularımız, bu yolun aktive olmasının uzuv yenilenmesinin erken evrelerinin başlatılmasında kritik bir rol oynadığını gösteriyor.
Uzuvlarını yenileyebilen hayvanlarda ise bu genin oksijen seviyelerine karşı daha az hassas olduğu ve geniş bir oksijen aralığında aktif kalabildiği görülüyor.
Çalışmada öne çıkan en çarpıcı bulgulardan biri ise HIF1A proteininin rolü.
Bu proteinin stabilize edilmesiyle birlikte hücrelerde erken evre yenilenme programlarının devreye girdiği görüldü.
Sadece uzuv değil, tüm doku onarımı
Elde edilen bulgular yalnızca uzuv yenilenmesiyle sınırlı değil.
Aynı mekanizmanın yara iyileşmesi ve bazı hastalık süreçleri için de önemli olabileceği belirtiliyor.
Aztekin şunları söyledi:
Oksijen seviyesinin düşürülmesinin bazı dokularda faydalı olabileceği daha önce de gösterilmişti. Örneğin kalp rejenerasyonu bağlamında düşük oksijenin olumlu etkileri olduğu biliniyor. Ancak bu etkiler şimdiye kadar büyük ölçüde metabolik değişimler üzerinden yorumlanıyordu. Bu nedenle metabolizmayı hedefleyen tedavi yaklaşımlarının geliştirilmesi ön plana çıkıyordu.
Bizim bulgularımız ise bu etkinin yalnızca metabolizma ile sınırlı olmadığını; aynı zamanda hücrelerin mekanik özelliklerini ve epigenetik durumunu da etkilediğini gösteriyor. Bu da farklı mekanizmaları hedefleyen daha geniş bir tedavi yaklaşımı yelpazesinin düşünülebileceğine işaret ediyor.
Yeni bir dönemin kapısı mı?
Uzuvların kısa vadede yeniden büyütülmesi mümkün görünmese de bu mekanizmanın anlaşılması bilim dünyasında önemli bir kırılma noktası olarak değerlendiriliyor.
“Bizim araştırmalarımız şu an için temel bilim düzeyinde" diye belirten Aztekin, ayrıca şu bilgileri verdi:
Şu ana kadarki çalışmalarımız embriyonik farelerde ve rejenerasyonun erken evrelerine odaklandı. Yetişkin dokularda ve yenilenmenin ileri aşamalarında neler olacağını henüz bilmiyoruz. Bu nedenle bulgularımızın ne zaman insanlar için uygulamalara uyarlanabileceğini öngörmek şu aşamada oldukça zor.
Bununla birlikte memelilerde uzuv yenilenmesi şimdiye kadar çoğunlukla bilim kurgu olarak görülüyordu. Bizim bulgularımız ise bunun tamamen ulaşılamaz bir hedef olmadığını ve belirli biyolojik mekanizmalar üzerinden mümkün olabileceğini somut bir şekilde ortaya koyuyor. Bu nedenle bu çalışmayı bir başlangıç olarak görüyoruz.
*Bu içerik serbest gazeteci veya konuk yazarlar tarafından hazırlanmıştır. Bu içerikte yer alan görüş ve ifadeler yazara aittir ve Independent Türkçe'nin editöryal politikasını yansıtmayabilir.
© The Independentturkish